我国口服复杂制剂市场情况分析 | 研发水平快速提升 国产替代持续推进
发布日期:2022-09-24 阅读次数:9764 来源:中国食品药品网
摘要:
目前,我国口服复杂制剂的研发水平已经基本跟上国际步伐,在改良型创新产品的申报上,我国的审评要求更加严格。随着辅料和制剂工艺的快速发展,部分口服复杂制剂的生产比一些难溶药物的普通口服制剂更易实现量产。
口服固体缓释制剂
当前,口服固体制剂的创新主要围绕提高难溶性药物的口服吸收率展开,如不断引入纳米晶等新技术来丰富口服药的吸收方式。传统的口服制剂口腔速崩片制备技术、口服缓控释技术、口服复方制剂和遮味技术已经难以称得上“高端”。以缓释技术为例,国内企业提供的解决方案多种多样,但在当前的市场环境下具有差异化的技术很难突出。如二甲双胍缓释片,青岛百洋医药、重庆康刻尔制药在生产中采用了渗透泵技术,但较高的研发和生产成本使其很难在集采中胜出,转而寻求院外市场。据国家药监局和国家药监局药品审评中心(CDE)有关数据,截至2022年4月初,我国已批准上市缓释制剂产品908个(按批准文号),处于审评阶段的受理号约有4400个。
根据样本医院数据,目前国内医药市场中缓释制剂重点品种主要包括琥珀酸美托洛尔缓释片、盐酸羟考酮缓释片、非洛地平缓释片、盐酸文拉法辛缓释胶囊、盐酸哌甲酯缓释片、帕利哌酮缓释片、格列齐特缓释片、单硝酸异山梨酯缓释片、洛芬待因缓释片、长春胺缓释胶囊、头孢克洛缓释片(Ⅱ)、甲磺酸多沙唑嗪缓释片、美沙拉秦缓释颗粒等20个品种。根据样本医院数据测算得到的上述重点品种2021年全国市场规模总和(以下简称推总规模)约为180亿元,2012—2021年的年复合增长率(CAGR)为5.9%。其中,2021年较2020年增幅趋缓,仅为1.1%,预计2025年前后市场规模将达200亿元。在20个重点品种中,琥珀酸美托洛尔缓释片2021年推总规模最大,为30.14亿元;2012—2021年CAGR最高的为甲磺酸多沙唑嗪缓释片,为115.58%,同时该品种2021年市场规模较2020年增长2.6倍以上;2021年推总规模排在前5名的产品中,盐酸羟考酮缓释片、盐酸文拉法辛缓释胶囊这两个品种较2020年略有下降。
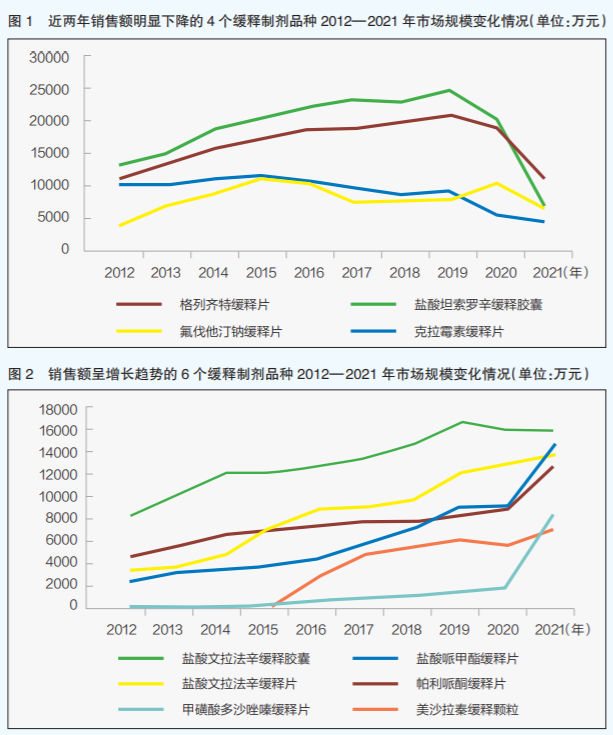
样本医院数据显示,近几年受药品集采影响,格列齐特缓释片、盐酸坦索罗辛缓释胶囊等品种年销售额出现大幅下滑(详见图1);而盐酸文拉法辛缓释胶囊、盐酸哌甲酯缓释片等品种年销售额出现明显增长(详见图2)。
口服控释制剂
我国对控释制剂的审批较为严格。笔者根据国家药监局网站数据统计发现,目前在我国获批上市的控释制剂品种仅有5个,分别为广州一品红、合肥立方、青岛百洋、海南先声、上海现代、南京易亨、北京红林、拜耳等企业生产的硝苯地平控释片,意大利Savio Industrial S.r.L.公司生产的卡左双多巴缓释片(早期批准时为控释片),北京中惠、常州四药生产的硫酸沙丁胺醇控释片,南京易亨、常州四药、辉瑞、淄博万杰、北京红林等企业生产的格列吡嗪控释片,广东百澳生产的盐酸地尔硫控释胶囊(180mg、150mg、120mg、90mg)。
从市场竞争格局来看,硝苯地平控释片市场长期由拜耳的产品主导,现有国产品种所占市场份额不足5%,但近年来新进入药企正逐渐撬开市场缝隙,未来随着集采步伐的加快,该产品的主流医院市场格局有望改变。盐酸地尔硫控释胶囊主要由广东百澳占据国内医药市场,但由于该品市场表现一般,后续跟进的企业并不多。对于格列吡嗪控释片,目前国产品种所占市场份额接近四成,对辉瑞产品的替代步伐正在加快。
据笔者统计,2015年1月至2022年4月,共有9个控释制剂产品在我国进行不同类型的申请,相关申请(包括仿制申请、进口申请、新药注册申请、补充申请等)共70个。其中,60个申请与硝苯地平控释片、格列吡嗪控释片有关;越洋医药有3个上市申请,均围绕2.2类控释产品苯磺酸氨氯地平控释片开展;拜耳的申请为1类新药BAY1101042钠控释片的上市申请,这是一款新型可溶性鸟甘氨酸环化酶(sGC)激动剂,是通路中关键的信号转导酶,可参与抑制细胞增殖和血小板聚集、舒张血管等一系列生理或病理反应;万邦德对石杉碱甲控释片进行了2.2类新药上市申请;上海汉都对卡左双多巴控释片进行了2.2类新药上市申请;青岛百洋对已上市产品盐酸二甲双胍控释片进行了补充申请。
硝苯地平控释片、格列吡嗪控释片是当前的竞争热点。从2012—2021年样本医院销售情况来看,硝苯地平控释片销售额稳定上行,格列吡嗪控释片销售额整体趋稳但稍有下滑(详见图3)。
口服速释制剂
采用速释技术的药品有很多,而口崩片是目前国内该领域的主要代表。2005年以来,我国陆续批准上市的口崩片产品有113个文号80余个品规。其中,冻干口崩片的速释效果更明显,部分冻干口崩片产品崩解更快、口感更好,但在与同名称非冻干口崩片的竞争中难以脱颖而出。
目前口崩片整体市场规模较小,发展高峰时期高端医院市场推总规模接近5亿元,而目前仅有3亿元左右。主要原因为该类型产品总体接受程度不高。同时,市场受一两个产品的销售波动影响较大。非冻干口崩片长期占据绝大部分的市场份额,近年来,冻干口崩片逐渐被市场接受,但份额增长依旧缓慢。
精神神经类药物是最容易被市场接受的一类口崩药物,其中米氮平、氯氮平、利培酮、唑吡坦等表现相对突出。尤其是米氮平口崩片,长期以来在口崩片市场占据较大份额,远超其他产品(详见图4)。这些领先产品的仿制跟进企业不多,从数据上看,自2015年以后口崩产品共有50多个仿制申请被受理。其中,奥氮平有21个,西地那非和阿立哌唑各有8个,是目前口崩产品的仿制热点。
笔者认为,口崩片尤其是冻干口崩片生产成本较高,因此该类药物带来的益处在国内主要被精神神经类疾病治疗领域适度接受,在其他领域的应用拓展依然任重道远。
相关链接
创新复杂制剂“扩张”潜力显现
BCC Research的研究报告显示,全球创新复杂制剂市场规模将从2020年的2310亿美元增长到2025年的3100亿美元,2020—2025年的年复合增长率预计为6.1%。按2020年全球医药市场规模1.2万亿美元计算(按出厂价统计),创新复杂制剂的销售收入占全球医药市场接近两成的份额(占比19.25%)。对比2020年全球仿制药市场规模的4116亿美元,以及2020—2025年仿制药市场规模的年复合增长率9.6%,创新复杂制剂均有所不及。
不过,不同于仿制药的激烈竞争和迅速迭代,创新复杂制剂品种往往具有较长的生命力。代表性产品有:1989年在美国获批上市的日本武田制药注射用醋酸亮丙瑞林微球长效制剂,至今每年销售额仍有十几亿美元,该产品已从每月使用一次的长效微球发展成为每三个月或六个月使用一次的超长效制剂;由美国Al za公司(后被强生收购)开发并于1995年获美国食品药品管理局(FDA)批准上市的Doxil,是全球第一个获批上市的PEG化长循环脂质体(2003年由西安杨森引入中国市场),取得了长期较好的市场回报;由拜耳开发的硝苯地平渗透泵控释片也是长盛不衰的经典产品。
如今,创新复杂制剂仍然是延续产品生命力、创造新型市场的利器。根据FDA网站信息,2021年FDA共批准几十个新型制剂产品。其中,代表性产品之一Fyarro(西罗莫司白蛋白结合型纳米颗粒),是西罗莫司的一种新型制剂,被批准用于治疗局部晚期不可切除性或转移性血管周围上皮样细胞瘤成人患者;另一个代表性产品Zynrelef缓释液,是由局部麻醉剂布比卡因和低剂量非甾体类抗炎药美洛昔康组成的复方固定剂量组合产品,被批准用于提供某些术后长达72小时的疼痛缓解作用。随着对上市药物在临床中应用的反馈和研究,开发新型给药系统以弥补药物在临床使用中缺陷,是当前和未来改良型复杂制剂主要的研究方向,将给企业带来巨大的市场增长空间。
相关新闻
美欧日医疗器械监管法律制度概览与思考
2000年,中华人民共和国国务院令第276号公布了《医疗器械监督管理条例》(以下简称《条例》),构建了医疗器械法律制度的框架,我国医疗器械走上了依法治理的轨道。此后《条例》历经多次修订和修改。2021年施行的新版《条例》贯彻“四个最严”要求,全面落实党中央、国务院关于医疗器械审评审批制度改革精神,为鼓励医疗器械产业创新高质量发展提供了坚实的法治保障。
10808个小时之前
最畅销的基因与细胞疗法TOP10盘点
2017年是细胞和基因治疗领域具有里程碑意义的一年,在这一年里,美国食品和药品监督管理局(FDA)批准了首款CAR-T细胞疗法(Kymriah)上市,还批准了首款AAV基因疗法(Luxturna)上市。
11150个小时之前
检查员说 | 浅谈药物警戒检查后企业整改常见问题及解决办法
自2021年12月1日《药物警戒质量管理规范》(以下简称GVP)实施后,截至2023年底,笔者所在的北京市药品不良反应监测中心针对药品上市许可持有人开展了107家次GVP符合性检查。检查员在督促企业整改过程中,常常发现企业不能一次性完成整改,一些问题不能及时纠正,大大降低了检查整改工作效率。现对药物警戒检查后企业整改后出现的常见问题进行梳理并提出相关建议。
11150个小时之前
降脂“药王”缩水76亿,3款新药大涨超100%!海正、鲁南、京新独家产品突围
血脂调节剂是心脑血管系统药物中重要的品类之一,也是首批被国采盯上的临床常用药物。经历了国采五年时间,该类药物的市场规模大幅缩水,2020年至今在中国公立医疗机构终端已无百亿品种,新上市产品则持续爆发活力。2023年信达生物的托莱西单抗注射液获批,成为近年来首个上市的血脂调节剂生物药1类新药,打破了进口药独占市场的局面,君实、康方、恒瑞的PCSK9抑制剂正在冲刺上市,国内血脂调节剂市场又将迎来新局面。
11263个小时之前
中药企业爆发了!28家研发费用超84亿,天士力、以岭、康缘领跑,猛攻4200亿市场
11263个小时之前