生物类似药的命名及可互换性
发布日期:2022-08-01 阅读次数:11707 来源:中国医药报
摘要:
生物类似药具有复杂性,其在欧洲、美国、中国等国家和地区的发展历程存在很大不同。同时,各个国家和地区的政府部门对生物类似药的监管要求和尺度也有很大区别。例如,在生物类似药的可互换性和命名上,美国和欧洲的要求就不一致,这也进一步影响了生物类似药对原研药的替代率和处方渗透率。
命名规范有利于保障药品可追溯
药品名称包括通用名和商品名。对生物类似药名称进行规范管理有利于医生处方和患者用药,更重要的是利于药品上市后的药物警戒,利于监测可能出现的不良反应和其他安全性问题,确保药品的可追溯性。
在欧盟,生物类似药和化学仿制药一样,可以使用独特的商品名称和与其参照药相同的通用名(也称国际非专利名称,简称为INN)。例如,三星生物的生物类似药Benepali(商品名)的原研药是安进公司的Enbrel(商品名),都使用依那西普(Etanercept)作为通用名。
2017年1月,美国食品药品管理局(FDA)制定了《生物制品非专利名命名行业指南》。该指南规定,所有生物制品均应具备专有名称,由通用名(INN)和后缀4个小写字母组成,但该后缀必须是没有任何意义的(至少有3个字母不同)。此命名原则适用于既往或最近经《公共健康服务法》351(a)或351(k)批准的原研生物制品、相关生物制品和生物类似药。
FDA要求采用上述可区分后缀的原因包括以下两点:一是降低处方或药房配药错误的风险;二是将不良事件与特定相关产品进行准确关联,以便于实施有效的药物警戒管理。例如:2015年FDA批准了首个生物类似物Zarxio(商品名),该药物由诺华旗下山德士(Sandoz)生产。原研药是安进生产的Neupogen(商品名),其通用名是Filgrastim。按照FDA的规定,山德士在这个药的非专利名称后面加上了后缀“-sndz”,也就是Filgrastim-sndz。
可互换性成争论热点
目前,关于生物类似药的争论已经从监管法规的适当性转移到了可互换性的实践。可互换性是医疗专业人员及患者非常关心的一个问题,在美国和欧洲存在着不同的定义和监管框架。在欧洲,欧洲药品管理局(EMA)规定,可互换性是用一种预期具有相同临床效果的药物代替另外一种药物的可能性,这包括用一个生物类似药代替参照药(或相反)或者生物类似药之间的替换。EMA并没有对生物类似药的可互换性使用进行推荐。
在美国,一个可互换性产品的推出是通过相关的可互换性法规进行监管的,需要经专门的互换性临床研究进行验证。一种具有可互换性的生物类似药是可以由药剂师根据所在州政策进行替换的,且不会受到原始处方的干扰。2019年5月,FDA进一步发布了《可互换性生物类似药的审评指南》,规定生物类似药需要通过多次与原研药的交叉临床试验来证明其可互换性。获得可互换性资格的生物类似药可以用于对患者正在使用的原研药进行替换使用,并可获得一年的市场独占期。尽管FDA的指导意见发布不久,但美国大多数州已经制定了相关的州法律,以推动生物类似药替代原研药。
在医学界存在的一个关键问题是,生物类似药是否适用于已经接受原研药治疗的患者转换为生物类似药治疗。目前的互换性研究结果并不能证明用生物类似药替换参照药对安全性和有效性产生不良影响,因此,对可互换性的担心还停留在理论阶段,且这些担心背后的科学依据还并不清楚。
互换性研究不太可能解决诸如“从一种生物类似物转换到另一种生物类似物是否安全”之类的问题。欧洲监管部门没有将可互换性研究作为生物类似药审批的一部分而提出强制要求。但一些处方医生还是希望,在患者从参照药治疗转换为生物类似药治疗之前,有必要进行互换研究。然而,如果要求进行涵盖临床实践中所有情况的互换研究,很可能会抵消生物类似药开发的成本节约并阻碍生物类似药进入市场。此外,主要使用生物类似药的国家和地区可能缺乏支持从生物类似药转回原研药或从市场领先的生物类似药转到下一个生物类似药的互换研究。要求进行转换研究意味着第一个生物类似药可能在相当长的一段时间内在市场上占据主导地位,从而减少了竞争。
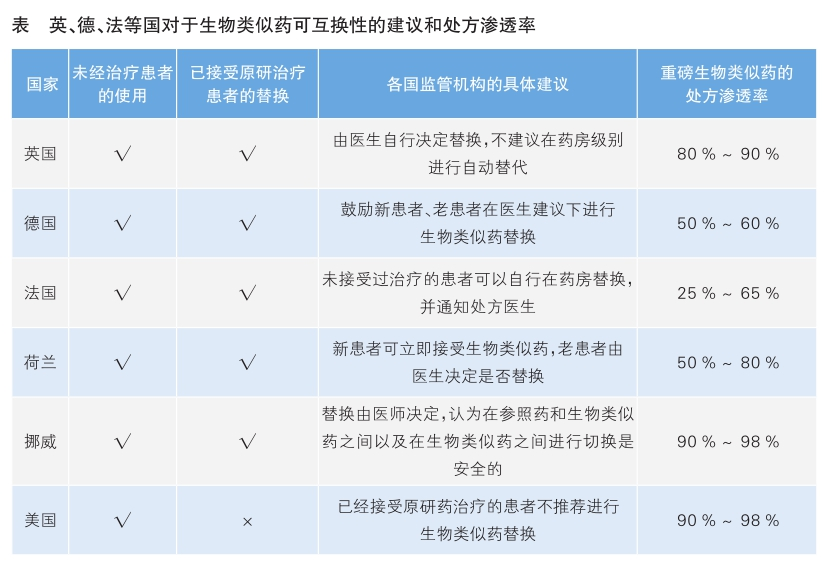
出于以上原因,医疗专业人士和政策制定者必须对生物类似药在可互换性方面的未经证实的理论风险和由于生物类似药竞争获得的成本节约进行权衡。现在做出决定是非常困难的,实际上,美国及欧洲部分国家在生物类似药可互换使用上的具体建议也不尽相同(详见表)。例如,美国对于已经接受原研药治疗的患者不推荐进行生物类似药转换,这大大影响了重磅生物类似药的处方渗透率(5%~20%),该数据远低于没有这种限制的欧洲国家。尽管如此,随着时间的推移,在强有力的科学证据支持下,进一步接受生物类似药的替换依然值得期待。
相关新闻
医学科普,听得懂更要讲得对
新一轮科技革命推动医学科技迅速发展,新装备、新技术、新药、新方案等已深度影响“促、防、诊、控、治、康”各环节,这也为健康科普提供了高水平的传播内容和传播载体。医学科普是以通俗易懂的方式将健康领域的科技知识、科学方法、科学思想和科学精神传播给公众,旨在培养公众的健康素养,帮助公众学会自我健康管理的长期性活动。建设健康中国,医学科普工作具有重要意义和独特作用。
11666个小时之前
推进中医药非遗传承保护
中医药非物质文化遗产(以下简称“中医药非遗”)是中华优秀传统文化的重要载体,亦是我国非物质文化遗产的重要组成部分。
12010个小时之前
基于质量源于设计路线的生物类似药质量研究
26714个小时之前
浅谈AI技术在COVID-19诊疗中的应用
26881个小时之前
“OK镜”市场迎来变数 疗效及安全备受关注
26881个小时之前














