创新药出海势在必行,砥砺前行
发布日期:2022-05-30 阅读次数:12822 来源:BCG波士顿咨询
摘要:
上篇介绍了中国药企全球化的总体趋势与挑战,看到创新药企和转型药企不约而同地增加创新药全球化布局。创新药的研发和出海似乎是谋求长远发展的共同选择,其背后的动因是什么?当前中国创新药国际化发展的现状是什么?
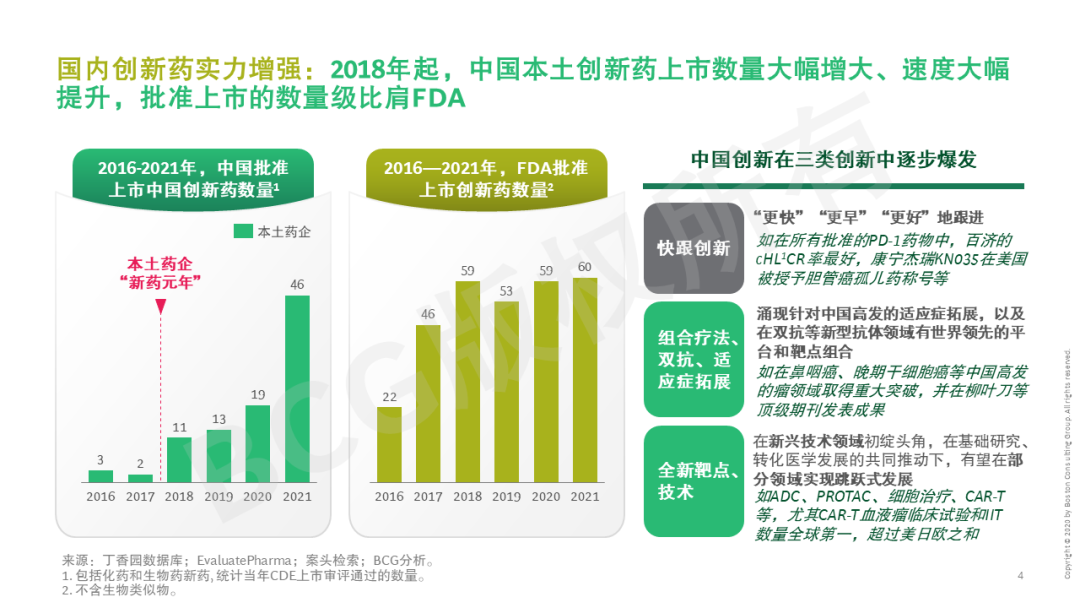
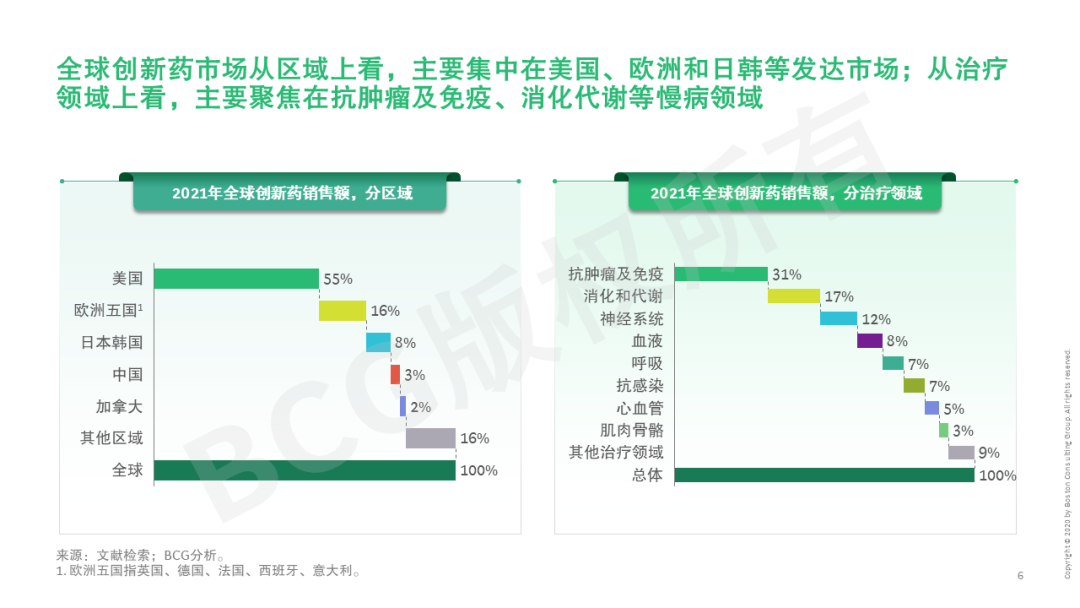
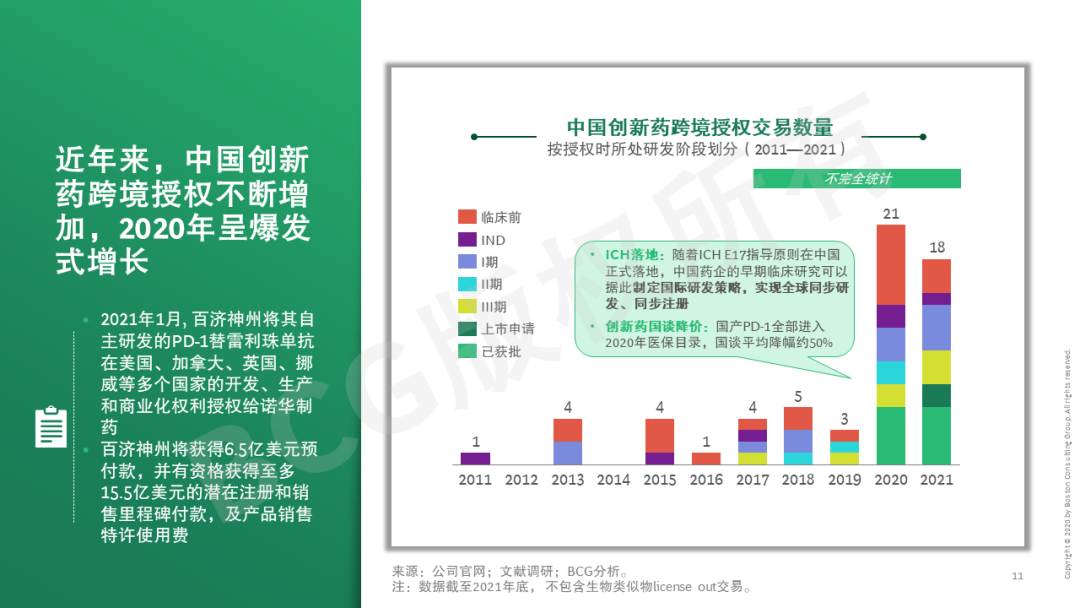
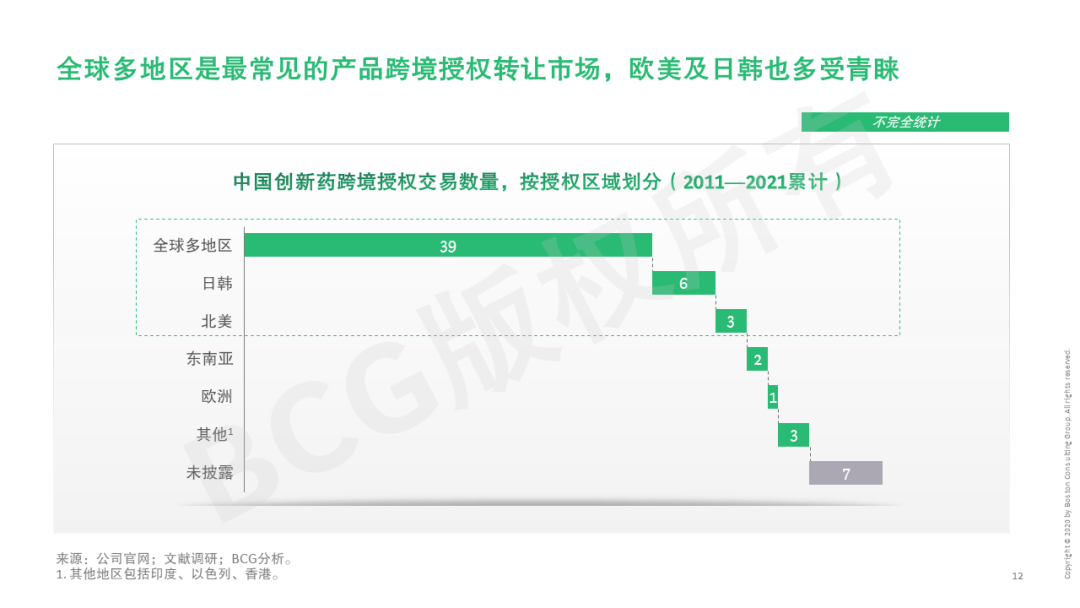
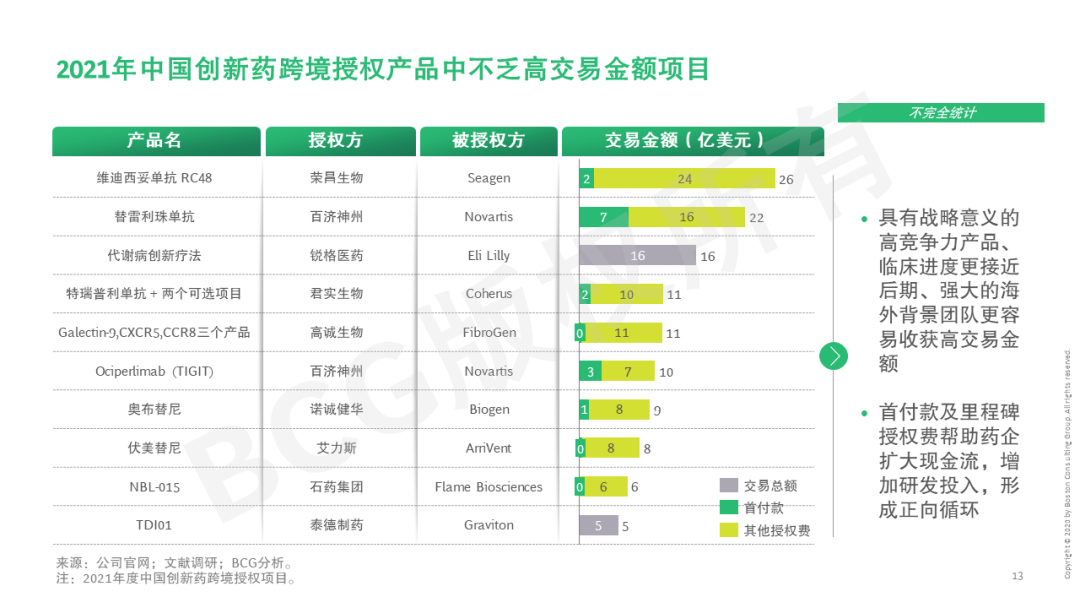
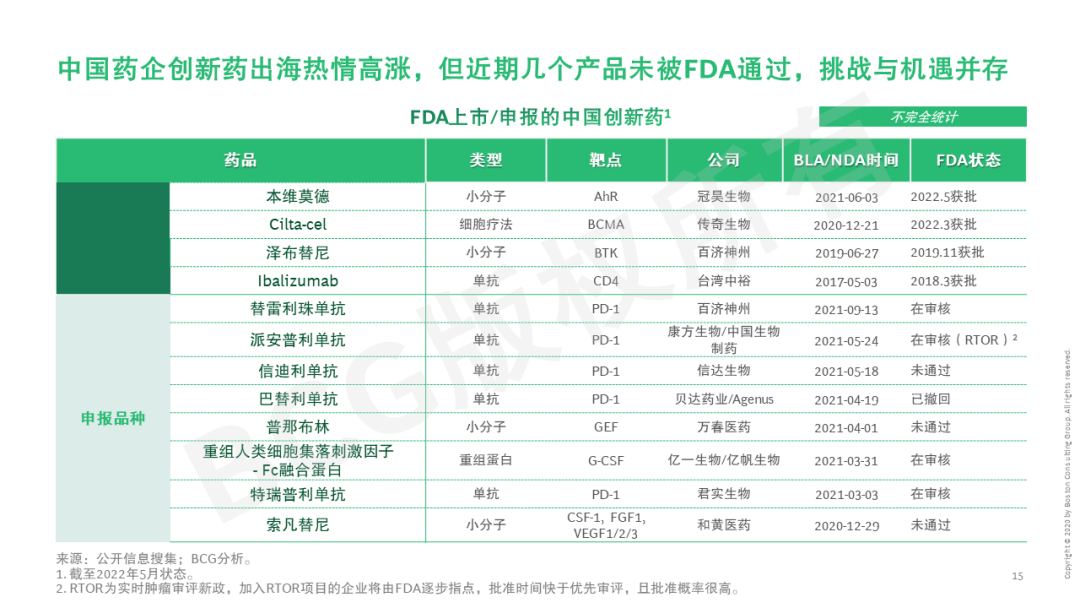
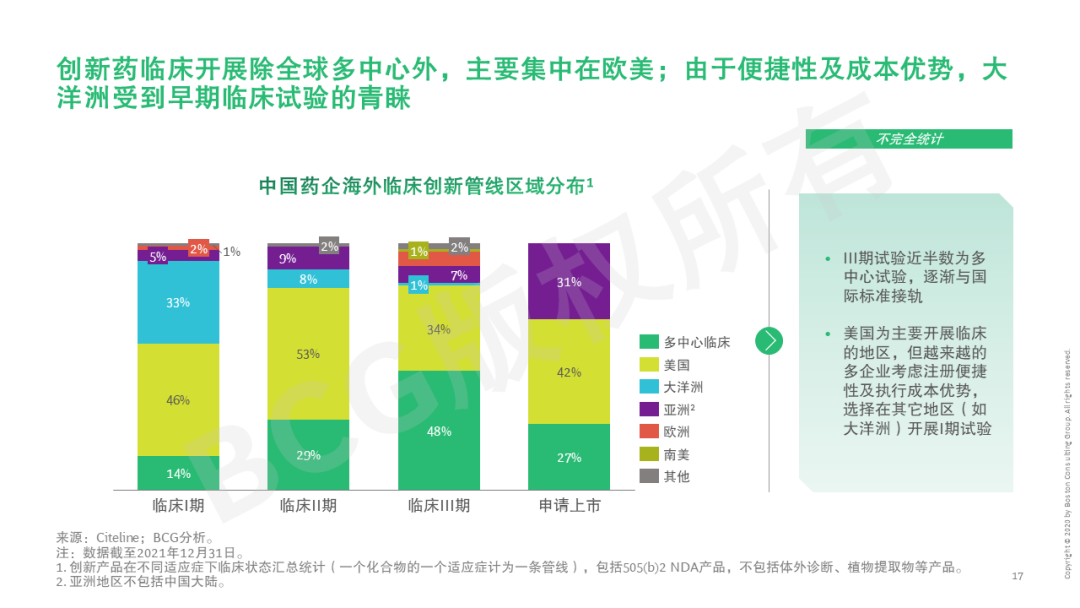
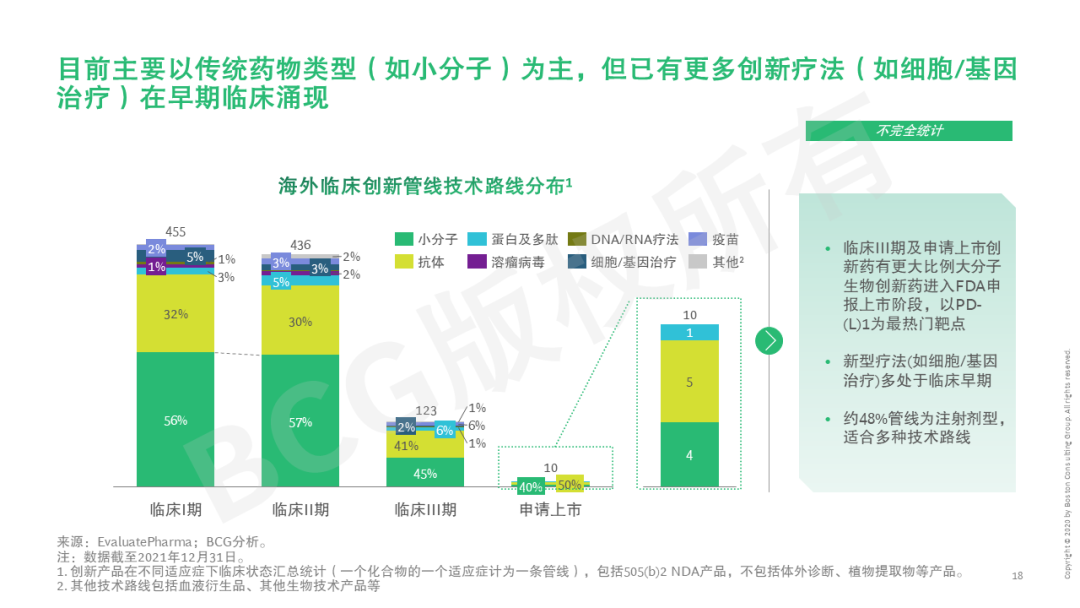
本系列第二篇文章将立足创新药,首先剖析市场和能力双轮驱动创新药国际化势在必行——国内创新实力增强、海外创新药市场吸引力大、而国内市场竞争激烈,同时中国创新药研发项目和人才、以及国际监管逐步与国际接轨。中国创新药近年来海外临床和授权交易已如雨后春笋般快速发展,本文也将探讨中国创新药出海聚焦的目标市场、技术路线、治疗领域等。近期,信迪利单抗、索凡替尼、普那布林等多个国内创新药未被FDA通过。今年5月20日,美国国会议员致信FDA局长和国会问责委员会GAO,对中国企业临床数据的人种多样性和临床试验质量再次提出质疑。这些对中国药企的全球临床试验能力提出更多挑战。但短期的挫折不会影响创新药出海的大势所趋,反而是提升药企研发能力的好机会。披荆斩棘破万难,守得云开见月明。望对中国药企有所启示。
本系列共由五篇文章组成:
创新药出海动因和趋势
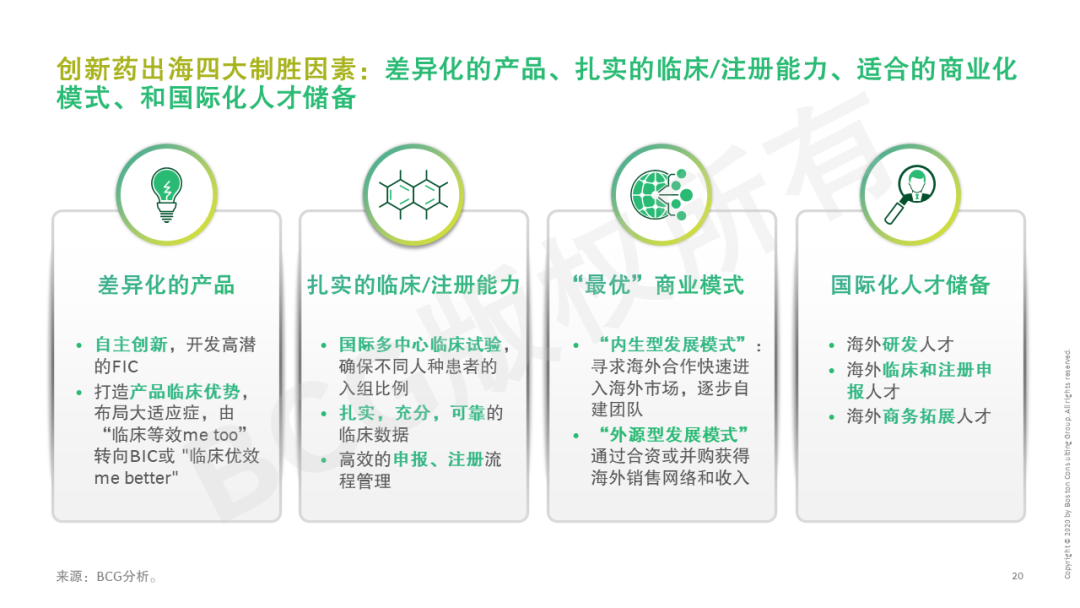
创新药出海模式
仿制药出海动因和趋势
出海需具备的组织能力













相关新闻
美欧日医疗器械监管法律制度概览与思考
2000年,中华人民共和国国务院令第276号公布了《医疗器械监督管理条例》(以下简称《条例》),构建了医疗器械法律制度的框架,我国医疗器械走上了依法治理的轨道。此后《条例》历经多次修订和修改。2021年施行的新版《条例》贯彻“四个最严”要求,全面落实党中央、国务院关于医疗器械审评审批制度改革精神,为鼓励医疗器械产业创新高质量发展提供了坚实的法治保障。
11422个小时之前
最畅销的基因与细胞疗法TOP10盘点
2017年是细胞和基因治疗领域具有里程碑意义的一年,在这一年里,美国食品和药品监督管理局(FDA)批准了首款CAR-T细胞疗法(Kymriah)上市,还批准了首款AAV基因疗法(Luxturna)上市。
11764个小时之前
检查员说 | 浅谈药物警戒检查后企业整改常见问题及解决办法
自2021年12月1日《药物警戒质量管理规范》(以下简称GVP)实施后,截至2023年底,笔者所在的北京市药品不良反应监测中心针对药品上市许可持有人开展了107家次GVP符合性检查。检查员在督促企业整改过程中,常常发现企业不能一次性完成整改,一些问题不能及时纠正,大大降低了检查整改工作效率。现对药物警戒检查后企业整改后出现的常见问题进行梳理并提出相关建议。
11764个小时之前
降脂“药王”缩水76亿,3款新药大涨超100%!海正、鲁南、京新独家产品突围
血脂调节剂是心脑血管系统药物中重要的品类之一,也是首批被国采盯上的临床常用药物。经历了国采五年时间,该类药物的市场规模大幅缩水,2020年至今在中国公立医疗机构终端已无百亿品种,新上市产品则持续爆发活力。2023年信达生物的托莱西单抗注射液获批,成为近年来首个上市的血脂调节剂生物药1类新药,打破了进口药独占市场的局面,君实、康方、恒瑞的PCSK9抑制剂正在冲刺上市,国内血脂调节剂市场又将迎来新局面。
11877个小时之前
中药企业爆发了!28家研发费用超84亿,天士力、以岭、康缘领跑,猛攻4200亿市场
11877个小时之前














